| Главная » Статьи » Мои публикации |
СРАВНИТЕЛЬНАЯ ХАРАКТЕРИСТИКА УЛЬТРАСТРУКТУРНЫХ ИЗМЕНЕНИЙ ПЕЧЕНИ И ВЫБОР ХИРУРГИЧЕСКОЙ ТАКТИКИ ПРИ МЕХАНИЧЕСКОЙ ЖЕЛТУХЕ У ПОЖИЛЫХ БОЛЬНЫХ
РезюмеВ работе представлена сравнительная характеристи-ка ультраструктурных изменений печени при механической желтухе различной этиологии. Определены и детально описа-ны основные клинико-морфологические варианты обтурацион-ного холестаза. На гистологическом и электронно-микроскопическом уровнях доказано решающее значение син-дрома желчной гипертензии в развитии патологии печени при непроходимости желчных путей. Обоснован дифференцирован-ный подход к выбору методов хирургической коррекции пато-логии желчевыводящей системы в соответствии с этиологией, длительностью и интенсивностью желтухи. В зависимости от клинико-биохимической картины заболевания установлены и подтверждены морфологически критерии операционного риска, показания к ограничению объема операции и применению этапного хирургического лечения. Обоснована необходимость применения современных мембранопротекторов и изучены на уровне ультраструктур возможные мишени их воздействия. Изложен опыт фармакотерапии ксимедоном при механической желтухе. На основании литературных данных и собственного опыта предложены рекомендации применения ксимедона.
Ключевые слова: механическая желтуха, холестаз, электрон-ная микроскопия печени, ксимедон. Одной из актуальных проблем абдоминальной хирургии является выбор оптимальной тактики хирургического лечения обтурационного холестаза у больных пожилого и старческого возраста. Остаются дискутабельными вопросы сроков оперативной коррекции непроходимости желчных путей, объема операции, предварительного применения декомпрессии билиарной системы малоинвазивными методами [3,5,6]. Предложены многочисленные методы исследования функциональных возможностей печени, определения риска операции для оценки переносимости пациентом определенного объема вмешательства [9,11,13,14,17]. Тем не менее, имеется лишь немного трудов, где изучается зависимость операционного риска от морфологических изменений печеночной ткани [7,10,12]. Остается дискутабельной роль гепатопротекторов при механической желтухе, поскольку до сих пор применение их базировалось только на клиническом опыте без подтверждения морфологическими данными. Установлено, что оксидативный стресс имеет место при обтурационном холестазе, доказано его значение для течения послеоперационного периода [22]. Однако остается неясным, какие препараты следует применять при данной патологии с целью коррекции нарушений перекисного окисления липидов. В числе применяемых мембранопротекторов ряд препаратов обладают существенными недостатками, что ограничивает их использование. Например, глюкокортикоиды являются иммунодепрессантами, эффект эссенциале слабый, гептрал очень дорог и т.д. В последнее время в клинической практике все чаще используется ксимедон, обладающий свойствами гепатопротектора [1], иммуно-модулятора [2,20], антиоксиданта [4,19], стимулятора репаративных процессов [2], активатора тканевого дыхания, сопряженного с синтезом макроэргов [15], стабилизатора состояния SH-групп [16], ДНК [21] и многими другими важными свойствами [2,18].
Целью настоящей работы стало изучение основных отличий вариантов течения обтурационного холестаза в зависимости от выраженности синдрома желчной гипертензии, дли-тельности, интенсивности желтухи, ее этиологии и ультраструктурных изменений печени, а также морфологическое обоснование применения гепатопротекторов. В хирургическом отделении больницы №35 г. Нижнего Новгорода мы наблюдали за 14 лет 430 больных с синдромом механической желтухи, в том числе 312 пациентов пожилого и старческого возраста. Клиническую картину заболевания, биохимические и иммуно-химические анализы мы соотносили с результатами исследований биоптатов печени методами оптической и электронной микроскопии. На основании проведенной работы мы выявили несколько вариантов течения обтурационного холестаза, требующих различной лечебной тактики.
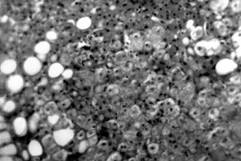
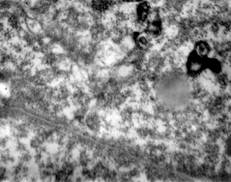
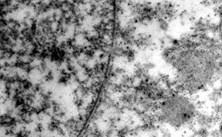
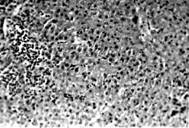
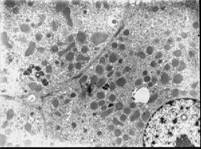
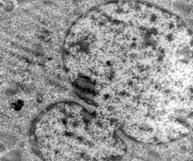
1. Ургентные больные с острым блоком желчных путей. Этио-логия заболевания – конкремент терминального отдела холедоха или множественный литиаз на фоне стеноза БДС, гной-ный холангит. У данной группы лиц на светооптическом уровне в течение 12–24 часов развивается дистрофия гепатоцитов, к 48 часам до гидропической и баллонной (Фото 1). На ультраструктурном уровне к 24 часам определяются патология митохондриальных мембран, к 48 часам – патология клеточной мембраны (Фото 2) и цитоплазматических структур и деструкция митохондриальных мембран (Фото 3); к 72 часам – нарушение целостности ядерной мембраны и элементы кариолизиса (Фото 4). Уровень билирубина может быть различным, но темп его нарастания около 100 мкмоль/л в сутки. Высокие уровни трансаминаз, ферритин 500 - 2000 нг/мл. В данной категории больных предпринимается немедленное оперативное вмешательство с полной одномоментной коррекцией непроходимости желчных путей.
3. Больные с длительной, интенсивной желтухой и манифестированной печеночной недостаточностью (более 20 суток, билирубин свыше 300 мкмоль/л, ферритин 4000 – 8000 нг/мл). Светооптически выявляется лимфогистиоцитарная инфильтрация перипортальных полей, фиброз, очаги некроза гепатоцитов. На ультраструктурном уровне практически тотальная деструкция цитоплазматических элементов, митохондрий, кариолизис (Фото 9). После предоперационной подготовки в течение 12–24 часов выполняется декомпрессивное вмешательство – холецистостомия из минидоступа в случае желчного пузыря in situ, пункционная холангиостомия под УЗИ – контролем, если пузырь удален ранее, либо имеется высокий билиарный блок. ЭПСТ противопоказана в большинстве случаев из-за риска кровотечения. Через 10 – 14 суток решается вопрос о втором этапе хирургического лечения.
4. Лица с желтухой небольшой интенсивности (до 100 мкмоль/л, ферритин 250 нг/мл) и давностью заболевания не более 7 суток. На светооптическом уровне – начальные фор-мы дистрофий гепатоцитов, на ультраструктурном – большинство мембранных комплексов сохранено, отмечается набухание митохондрий, неоднородность матрикса (Фото 10). Опе-ративное вмешательство в любом объеме, в случае необходи-мости дообследования может быть несколько отложено на фоне консервативной терапии, а в случая ее успеха операция выполняется после стихания желтухи чаще всего в объеме холецистэктомии из минидоступа с интраоперационной холангиографией.
Анализируя картину ультраструктурных изменений печени при механической желтухе, мы пришли к выводу, что степень патоморфологических сдвигов зависит от этиологии процес-са, тяжести холестаза и его продолжительности. При желтухе доброкачественного происхождения основным механизмом повреждения печеночных клеток и причиной развития острой печеночной недостаточности является феномен дистрофии. Пусковым фактором развития последней служит гипоксия клеток печени вследствие повышения внутрипротокового давле-ния и нарушений регионарной гистоперфузии. Этот механизм реализуется легко, так как механическая желтуха всегда сопровождается снижением системного печеночного кровотока (и венозного, и артериального), кроме того, любое хирургическое вмешательство ведет к снижению органной перфузии. Большинство анестетиков (кроме оксибутирата натрия) также индуцируют депрессию печеночного кровотока, поэтому одна из задач анестезиолога-реаниматолога состоит в обеспечении оптимальной органной перфузии и адекватной сис-темной оксигенации.
Через 48 часов при наличии ущемленного камня папиллы мы наблюдали тяжелые ультраструктурные изменения гепатоцитов. Наиболее быстро развивались повреждения мембран митохондрий (Фото 3) с развитием их некроза и образованием вторичных лизосом, затем повреждение клеточной мембраны с образованием “отверстий” (Фото 11), повреждение мембраны ядра клетки (Фото 4) с его некробиозом. Таким образом, при остром блоке билиарной системы имеется высокий риск повреждения мембранных комплексов гепатоцита, а значит, применение современных мембранопротекторов необходимо. При опухолевой обтурации протоков желчная гипертензия развивается постепенно, поражение печени часто является более тяжелым, чем при холедохолитиазе, но менее острым. Эти данные соответствуют результатам биохимических исследований - синдром цитолиза преобладает над синдромом холестаза при желтухе неопухолевого генеза. В целом степень повреждения биомембран зависит от выраженности желчной гипертензии и ее продолжительности. При медленном нарастании желтухи успевают развиться компенсаторные механизмы – деление клеток (Фото 8), элементы регенерации, относительно сохраненные структура и функция одних гепатоцитов (Фото 7) взамен деградирующих соседних клеток (Фото 6). В данном случае пациенту необходимо применение медикаментов, стимулирующих репаративные, регенераторные процессы. При интенсивной длительной желтухе наблюдается повсеместная гибель клеточных органелл и нуклеолизис (Фото 12). Прогноз послеоперационного периода в таких случаях весьма серьезный. Применение мембранопротекторов и стимуляторов регенерации возможно, однако большого эффекта ожидать не следует, так как практически отсутствуют основные мишени их воздействия. На основании данных электронной микроскопии мы сочли необходимым включение в лечебную программу больных с механической желтухой в до- и послеоперационном периоде современного препарата, обладающего свойствами мембранопротектора и стимулятора регенерации - ксимедона в дозе 2 г в сутки.
Применение ксимедона позволило расширить круг пациентов, которым может быть успешно выполнена радикальная одномоментная коррек-ция непроходимости желчных путей. Например, на электронограмме (Фото 13) мы видим все ведущие признаки тяжелой альтерации мембран гепатоцита у больного Б., 70 лет. На фоне терапии ксимедоном выполнена холедохолитотомия, холедоходуоденостомия по поводу механической желтухи и гнойного холангита, имел место гладкий послеоперационный период с нормализацией биохимических показателей в более короткие, чем обычно, сроки. Таким образом, активная хирургическая тактика при обтурационном холестазе и более частое применение этапного лечения малоинвазивными методами при механической желтухе опухолевого генеза являются морфологически обоснованными. С учетом данных электронной микроскопии печени при механической желтухе, применение гепатопротекторов (ксимедон) показано при выраженном синдроме желчной гипертензии, интенсивной длительной желтухе, гнойном холангите и абсолютно необходимо при острой обструкции желчных путей (ущемленный камень папиллы). Использование препарата позволяет существенно расширить круг лиц, которым может быть выполнена радикальная одномоментная коррекция непроходимости желчных путей.
В результате проведенных исследований мы пришли к следующим выводам. Главным фактором, определяющим срочность операции, является острота билиарного блока, выраженность синдрома желчной гипертензии, ведущего к нарушению регионарной гистоперфузии и тканевой гипоксии, деструкции энергетически значимых субклеточных структур. Звеном, определяющим результат лечения, является баланс между адекватностью восстановления проходимости желчных путей и степенью повреждения мембранных комплексов. Прогноз восстановления функции печени при тяжелой желтухе определяется соотношением структурно сохранных гепатоцитов и подвергшихся цито- и кариолизису. В лечебную программу у больного с механической желтухой следует включать современные гепатопротекторы, препаратом выбора является ксимедон.
ЛИТЕРАТУРА
| |||||||||
| Категория: Мои публикации | Добавил: surgeon (19.01.2008) | |||||||||
| Просмотров: 2997 | |||||||||
Категории каталога
| Мои публикации [47] |
|
Герниология [14]
Материалы по хирургическому лечению грыж
|
|
Панкреатология [10]
Все материалы по хирургии поджелудочной железы
|
| Послеоперационный период. Детская челюстно-лицевая хирургия. [3] |
Поиск
Наш опрос
| Copyright MyCorp © 2026 |
| Бесплатный хостинг uCoz |